Свойства оксидов
«Свойства солеобразующих оксидов»
Ключевые слова конспекта: свойства кислотных оксидов, свойства основных оксидов, свойства амфотерных оксидов.
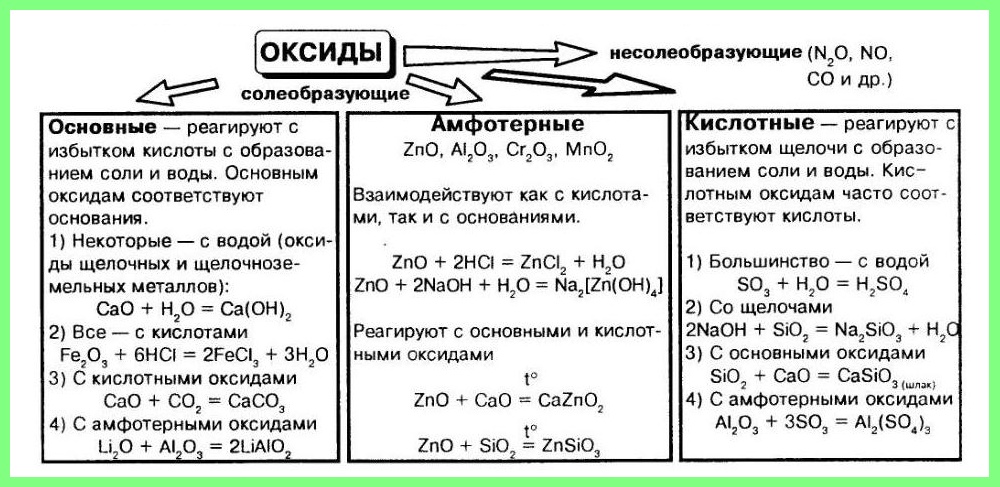
I. Свойства кислотных оксидов
1. Кислотные оксиды, кроме SiО2, реагируют c водой, образуя кислоту: CO2 + H2O → H2CO3
Чтобы составить формулу кислоты, нужно «сложить» все атомы исходных веществ, записывая на первом месте символ водорода, на втором — символ элемента, образующего оксид, и на последнем — символ кислорода. Если индексы получились чётными, их можно сократить: N2O3 + H2O → H2N2O4, или 2HNO2
Эти же реакции можно записать в виде «арифметического примера»:
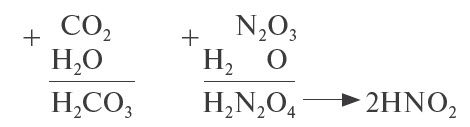
2. Кислотные оксиды реагируют с основными оксидами, образуя соль соответствующей кислоты, т. е. кислоты, которая образуется при взаимодействии этого оксида с водой (см. выше):
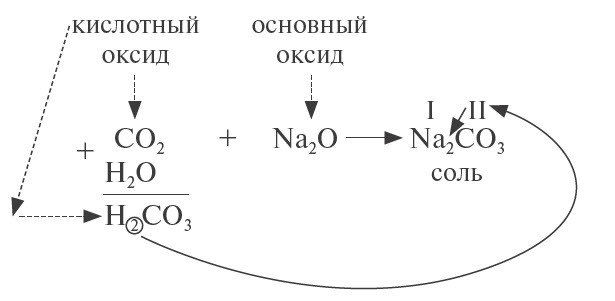
Для того чтобы составить такое уравнение, нужно:
- составить формулу кислоты («прибавив» к молекуле оксида молекулу воды);
- определить валентность кислотного остатка (это часть молекулы кислоты без атомов водорода). В данном случае кислотный остаток имеет состав СО3, его валентность равна числу атомов водорода в кислоте, т. е. II;
- составить формулу соли, записав вместо атомов водорода атом металла из основного оксида с его валентностью (в данном случае — натрий);
- составить формулу соли по валентности металла и кислотного остатка.
3. Кислотные оксиды реагируют с основаниями, образуя соль соответствующей кислоты и воду:
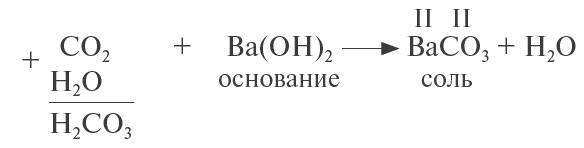
Принципы составления уравнения те же, что и для реакций с основными оксидами (см. пункт 2).
Кислотные оксиды и с кислотами и кислотными оксидами НЕ РЕАГИРУЮТ!
II. Свойства основных оксидов
- Основные оксиды реагируют с водой, образуя основание. Реакция происходит, если получающееся основание растворимо в воде.
Общая формула оснований Ме(ОН)х, где х — валентность металла, равная числу ОН групп.

Последняя реакция не идет, так как основание Fe(ОН)3 нерастворимо в воде. Растворимость веществ в воде можно определить по таблице растворимости.
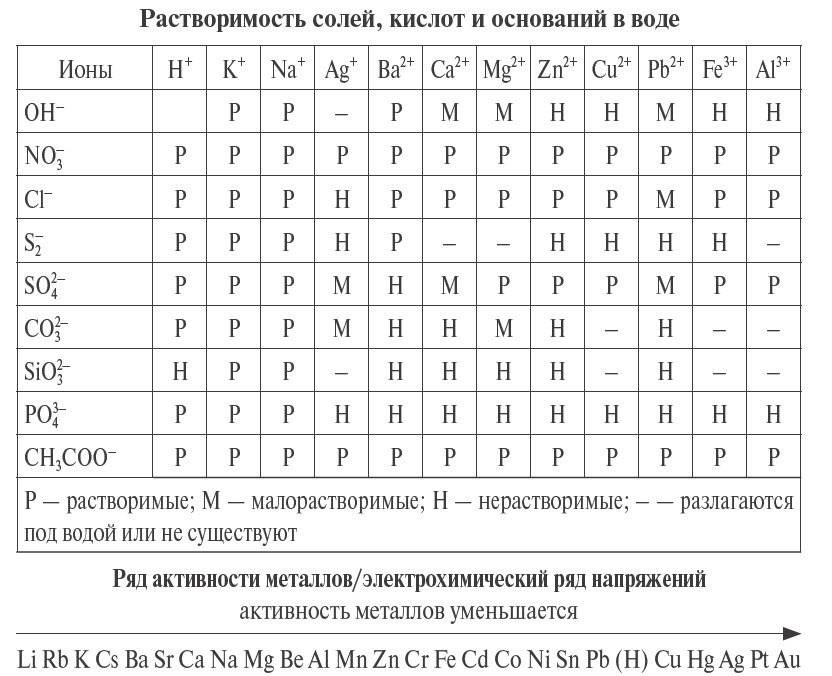
При определении возможности протекания данной реакции можно использовать и другое правило.
Основный оксид реагирует с водой, если он образован активным металлом. Такие металлы стоят в ряду напряжений до магния: Li K Ba Ca Na Mg …
- Основные оксиды реагируют с кислотами, образуя соль и воду:
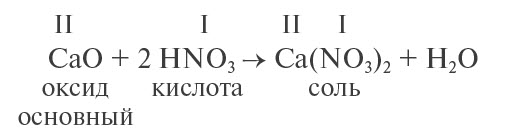
Обратите внимание: при составлении формулы соли нужно вместо атомов водорода в формуле кислоты написать символ металла, а затем составить полученную формулу по валентности.
- Основные оксиды реагируют с кислотными оксидами, образуя соль.
- Некоторые основные оксиды реагируют при нагревании с водородом, при этом образуется металл и вода:
CuO + H2 → Cu + H2O
Основные оксиды с основаниями и основными оксидами НЕ РЕАГИРУЮТ!
ВЫВОД. В реакцию легче всего вступают вещества с противоположными свойствами, и не вступают в реакцию вещества со сходными свойствами.
III. Свойства амфотерных оксидов
Амфотерные оксиды (от греч. amphi — двойной) проявляют двойственные свойства: они могут реагировать и с кислотами, и с основаниями (точнее, со щелочами). При этом образуются соль и вода.
Например,


Конспект урока «Свойства оксидов».
Следующая тема: «Основания».