Рябов Химия 8 Решение задач Химические понятия
Рябов Химия 8 Решение задач Химические понятия
Рябов Химия 8 Решение задач Химические понятия — это цитаты (задачи) из Главы 1 «Первоначальные химические понятия» пособия Сборник задач и упражнений по химии: 8-9 классы: к учебникам Г.Е. Рудзитиса, Ф.Г. Фельдмана «Химия. 8 кл.», «Химия. 9 кл». ФГОС (к новым учебникам) / М.А. Рябов. — М. : Издательство «Экзамен», 2016. А также ответы и решения задач из указанного сборника.
Цитаты из вышеуказанного учебного пособия использованы на сайте в незначительных объемах, исключительно в учебных и информационных целях (пп. 1 п. 1 ст. 1274 ГК РФ), при этом цитаты переработаны в удобный для пользователя формат. При постоянном использовании задач по химии в 8 классе необходимо купить книгу: Михаил Рябов: Химия. 8-9 классы. Сборник задач и упражнений. ФГОС / М.: Экзамен, 2018. Ответы и решения расчетных задач помогут родителям проверить правильность выполнения домашних заданий.
Ответы на расчетные задачи
1.120. Во сколько раз масса атома железа больше, чем масса атома кислорода?РЕШЕНИЕ:![]()
Ответ: в 3,5 раза.
1.137. В каком соотношении находятся числа атомов водорода и кислорода в молекуле воды? В каком массовом соотношении находятся водород и кислород в воде?
РЕШЕНИЕ:
Ответ: N(Н) : N(О) — 2:1, m(Н) : m(О) — 1:8.
1.138. Сколько граммов кислорода потребуется для сжигания 10 граммов водорода с образованием воды?
РЕШЕНИЕ:
Ответ: 80 г.
1.139. Каково соотношение чисел атомов железа и серы в сульфиде железа? Каково соотношение масс железа и серы в сульфиде железа?
РЕШЕНИЕ:
Ответ: N(Fe) : N(S) — 1:1, m(Fe) : m(S) — 7:4.
1.140. Железо соединяется с серой с образованием сульфида железа в соотношении масс 7 : 4. Сколько граммов железа потребуется для реакции:
а) с 12 г серы,
б) с 20 г серы?
РЕШЕНИЕ: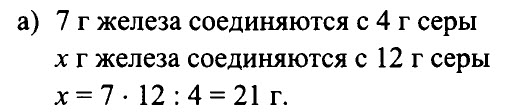
Ответ: a) 21 r, б) 35 r.
1.150. Определите относительные молекулярные массы следующих веществ:
а) воды Н20, б) сульфида железа FeS,
в) кислорода 02, г) хлорида натрия NaCl,
д) углекислого газа С02.
РЕШЕНИЕ:![]()
Ответ: a) 18, б) 88, в) 32, г) 58,5, д) 44.
1.161. Не производя вычислений, определите, в каком из оксидов массовая доля железа больше:
а) Fe304, б) FeO, в) Fe203.
Предположение подтвердите расчетом массовой доли железа в этих оксидах.
РЕШЕНИЕ: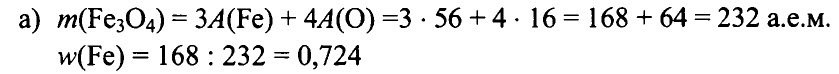
Ответ: FeO; a) 0,724, б) 0,778, в) 0,700.
1.162. Определите массовую долю водорода в следующих соединениях:
а) СН4, б) NH3, в) Н20, г) HF, д) HNО3.
РЕШЕНИЕ: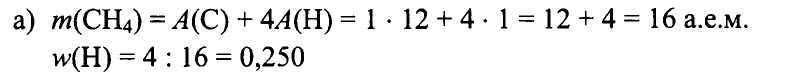
Ответ: a) 0,250, б) 0,176, в) 0,111, г) 0,050, д) 0,016.
1.163. Определите массовую долю кислорода в следующих соединениях:
а) СО2, б) NaOH, в) Н2О, г) СаСО3, д) HNО3.
РЕШЕНИЕ: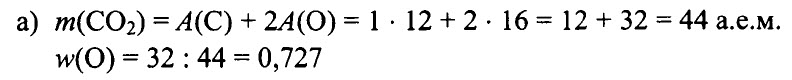
Ответ: а) 0,727, б) 0,400, в) 0,889, г) 0,480, д) 0,762.
1.164. Установите формулу вещества, содержащего …
а) 33,3% натрия, 20,3% азота и 46,4% кислорода,
б) 40,0% кальция, 12,0% углерода и 48,0% кислорода.
РЕШЕНИЕ: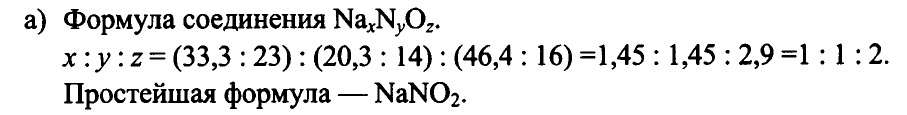
Ответ: a) NaNО2, б) СаСО3.
1.165. Установите формулу вещества, содержащего …
а) 55,2% калия, 14,6% фосфора и 30,2% кислорода,
б) 26,5% калия, 35,4% хрома и 38,1% кислорода.
РЕШЕНИЕ:
Ответ: а) К3РО4, б) К2Сг2О7.
1.219. Вычислите относительные молекулярные массы:
а) оксида меди(I), б) хлорида железа(II), в) оксида алюминия,
г) оксида марганца(IV), д) оксида фосфора(V), е) оксида серы(VI),
ж) оксида хлора(VII).
РЕШЕНИЕ:![]()
Ответ: а) 144, б) 127, в) 102, г) 87, д) 142, е) 80, ж) 183.
1.220. Вычислите массовые доли элементов в следующих соединениях:
a) FeCl3, б) SO2, в) N2O, г) NaCl, д) Cu2
РЕШЕНИЕ: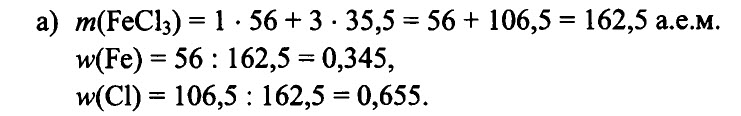
Ответ: а) 0,345 и 0,655, б) 0,500 и 0,500, в) 0,636 и 0,364, г) 0,393 и 0,607, д) 0,800 и 0.200.
Рябов Химия 8 Решение задач Химические понятия
Следующий раздел «Рябов Химия 8 Решение задач Кислород»